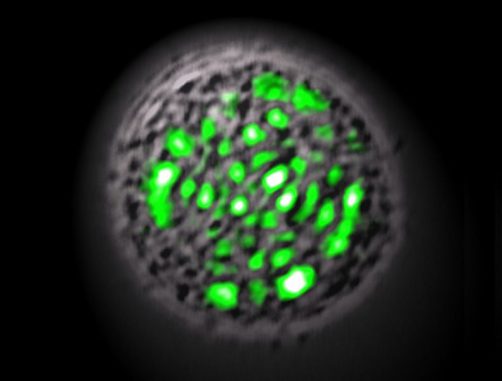
Es klingt wie etwas aus einem Comicheft oder einem Science-Fiction-Film – ein lebender Laser – aber genau das haben zwei Forscher des Wellman Center for Photomedicine am Massachusetts General Hospital entwickelt. In einer Abhandlung, die im Journal Nature Photonics erscheinen wird und online veröffentlicht wird, beschreiben die Wellman Forscher Dr. Malte Gather und Dr. Seok Hyun Yun, wie eine einzige Zelle benutzt werden kann, um die Lichtteilchen – Photonen genannt – zu nanosekundenlangen Impulsen aus Laserlicht zu verstärken. Die Zelle wurde genetisch modifiziert, um grün fluoreszierendes Protein (green fluorescent protein, GFP) herzustellen.
„Seit ihrer erstmaligen Entwicklung vor rund 50 Jahren haben Laser synthetische Materialien wie Kristalle, Farbstoffe und gereinigte Gase als optisches Verstärkungsmedium verwendet, in welchen die Photonenpulse durch das Vor- und Zurückprallen zwischen zwei Spiegeln verstärkt werden“, sagt Yun, Mitautor der Studie. „Dies ist der erste Bericht über einen funktionierenden biologischen Laser, der auf einer einzelnen, lebenden Zelle basiert.“
Gather, Forschungsstipendiat und der leitende Autor der Studie ergänzt: „Ein Teil der Motivation für dieses Projekt war wissenschaftliche Neugier. Weil biologische Substanzen keine große Rolle bei Lasern gespielt hatten, fragten wir uns, ob es einen fundamentalen Grund dafür gibt, dass Laserlicht soweit wir wissen nicht in der Natur auftritt und ob wir einen Weg finden könnten, Laser in biologischen Substanzen oder lebenden Organismen zu verwirklichen.“
Die Wissenschaftler wählten GFP für ihre Erforschung dieser Fragen, weil das Protein – ursprünglich in der Quallenspezies Aequorea_victoria entdeckt – dazu gebracht werden kann, Licht zu emittieren, ohne zusätzliche Enzyme anzuwenden. Seine Eigenschaften sind gut verstanden und es gibt etablierte Methoden, viele Organismen genetisch so zu programmieren, dass sie GFP produzieren. Um das Potenzial des Proteins zur Erzeugung von Laserlicht zu bestimmen, konstruierten die Forscher zunächst ein Gerät, das aus einem zentimeterlangen Zylinder mit Spiegeln an jedem Ende besteht und füllten es mit einer Lösung aus GFP in Wasser. Nach der ersten Bestätigung dafür, dass die GFP-Lösung zugeführte Energie zu kurzen Impulsen aus Laserlicht verstärken konnte, schätzten die Forscher, die GFP-Konzentration, die für die Erzeugung des Lasereffekts erforderlich war.
Unter Verwendung dieser Information bestand der nächste Schritt darin, eine Reihe von Säugetierzellen zu entwickeln, die die benötigten Mengen GFP produzieren. Der zelluläre Laser wurde zusammengesetzt, indem eine einzelne GFP-produzierende Zelle mit einem Durchmesser von 15-20 Millionstel Meter in einem winzigen Hohlraum aus zwei hochreflektiven Spiegeln platziert wurde, welche 20 Millionstel Meter voneinander entfernt waren. Das Zellbasierte Gerät erzeugte nicht nur Pulse aus Laserlicht wie in dem Experiment mit der GFP-Lösung, die Forscher fanden auch heraus, dass die sphärische Gestalt der Zelle selbst als Linse agierte, die das Licht refokussierte und die Emission von Laserlicht bei niedrigeren Energieleveln ermöglichte als für das Lösungsbasierte Experiment benötigt wurden. Die in dem Gerät benutzten Zellen überlebten den Laser-Prozess und waren in der Lage, mit der Erzeugung Hunderter weiterer Laserlichtimpulse fortzufahren.
„Während die einzelnen Laserimpulse nur wenige Nanosekunden dauern, sind sie hell genug, um sofort registriert zu werden und sie scheinen sehr nützliche Informationen zu enthalten, die uns neue Wege eröffnen könnten, die Eigenschaften einer großen Anzahl von Zellen augenblicklich zu analysieren“, sagt Yun, Dozent für Dermatologie an der Harvard Medical School. „Und die Fähigkeit, Laserlicht aus einer biokompatiblen Quelle innerhalb eines Patienten zu erzeugen, könnte für photodynamische Therapien nützlich sein, in denen Medikamente durch die Einwirkung von Licht oder neue Bildgebungstechniken aktiviert werden.“
Gather fügt hinzu: „Eines unserer langfristigen Ziele wird das Finden von Möglichkeiten sein, optische Kommunikation und Datenverarbeitung – zurzeit mit unbelebten elektronischen Bauteilen durchgeführt – in das Reich der Biotechnologie zu bringen. Das könnte insbesondere für Projekte zweckdienlich sein, welche die Verbindung von Elektronik mit biologischen Organismen erfordern. Wir hoffen auch, eine mit der winzigen Spiegelkammer vergleichbare Struktur direkt in eine Zelle implantieren zu können, was der nächste Meilenstein für diese Forschungsarbeit wäre.“ Die Studie wurde finanziell unterstützt von der National Science Foundation und der Korea National Research Foundation.
Quelle: http://www.eurekalert.org/pub_releases/2011-06/mgh-sgc061011.php
(SOM)
Antworten